特定臨床研究
【研究推進センター 臨床研究支援室(CRB担当)】![]()
はじめに ~規制法令・指針等の確認~
参考情報) 厚生労働省 > 臨床研究法について
臨床研究法の改正概要(説明資料 2025年6月)【PDF】
臨床研究法の概要【PDF】
臨床研究法の施行等に関するQ&Aについて【PDF】
該当性に関するチェックリスト1【PDF】
開始時手続きに関するチェックリスト【PDF】
1.COI(利益相反管理)
利益相反状況の確認は、概ね5名までで1週間、5名以上では2週間程度かかります。
参考情報) 厚生労働省 > COI(利益相反管理)について【PDF】
2.管理者実施許可手続き(院長決裁)
認定臨床研究審査委員会(CRB)で承認を得られましたら、「臨床研究実施許可に関する届出書(新規)」と共に承認書類一式をお送りください。
【確認事項】
● 用いる医薬品等が未承認・適応外に該当する場合は、未承認・禁忌・適応外医薬品等評価委員会や未承認等新規高度管理医療機器等評価委員会などに研究者より申請
● 臨床研究保険加入状況(女子医大で実施する場合には基本的に女子医大の病院が臨床研究保険でカバーされていることが必要です)
3.報告(疾病、不適合、定期報告等)手続き(院長報告)
認定臨床研究審査委員会(CRB)から報告事項がありましたら、書類一式をお送りください。
当院で疾病等が発生した場合
・疾病等報告
特定臨床研究に起因するものと疑われる疾病、傷害若しくは死亡又は感染症の発生状況を病院長、統括管理者及び承認を受けた認定臨床研究審査委員会に報告する
参考情報)厚生労働省 > 臨床研究法の統一書式について【PDF】 統一書式(8~10)【PDF】
当院で不適合と疑われる事例を知った場合
・不適合報告
臨床研究法における「重大な不適合」とは、臨床研究の対象者の人権や安全性及び研究の進捗や結果の信頼性に影響を及ぼすものをいう。例えば、選択・除外基準や中止基準、併用禁止療法等の不遵守をいう。
参考情報)報告フロー (出典 AMED)
参考情報)厚生労働省 > 臨床研究法の統一書式について【PDF】 統一書式(7)【PDF】
※(令和4年3月31日 医政研発 0331 第1号)実施医療機関の管理者は、当該「重大な不適合」に関する対応の状況等を公表すること。
4.各種手順書・様式(※学内専用(Box))
実施の流れ
↓クリックするとPDFファイルが開きます(※学内専用(Box))
| ◆当院が分担施設の場合の流れ | ◆当院が代表施設の場合の流れ |
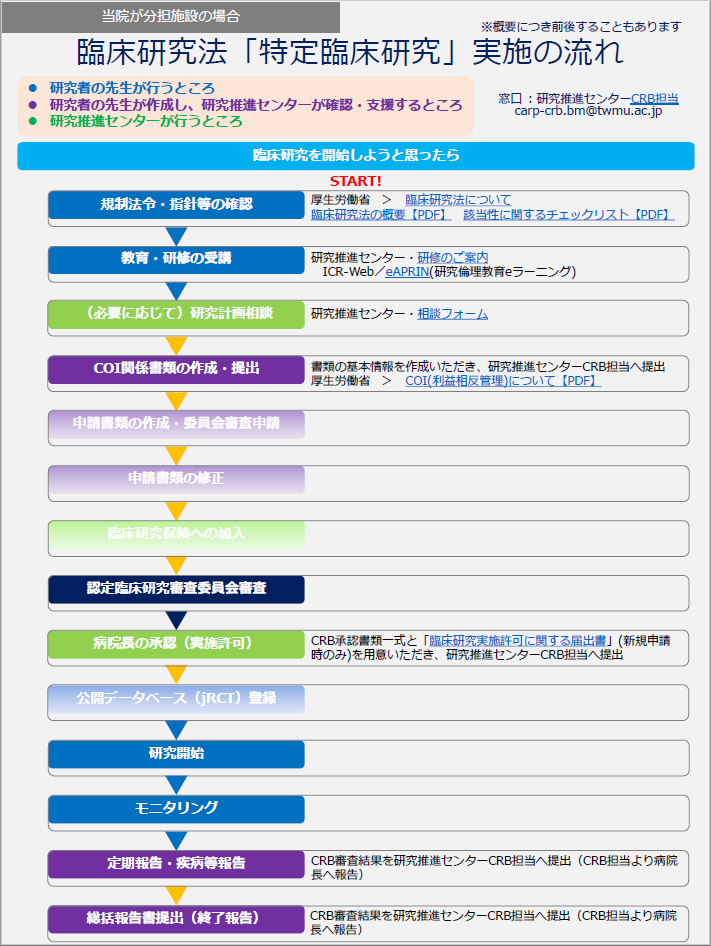
|
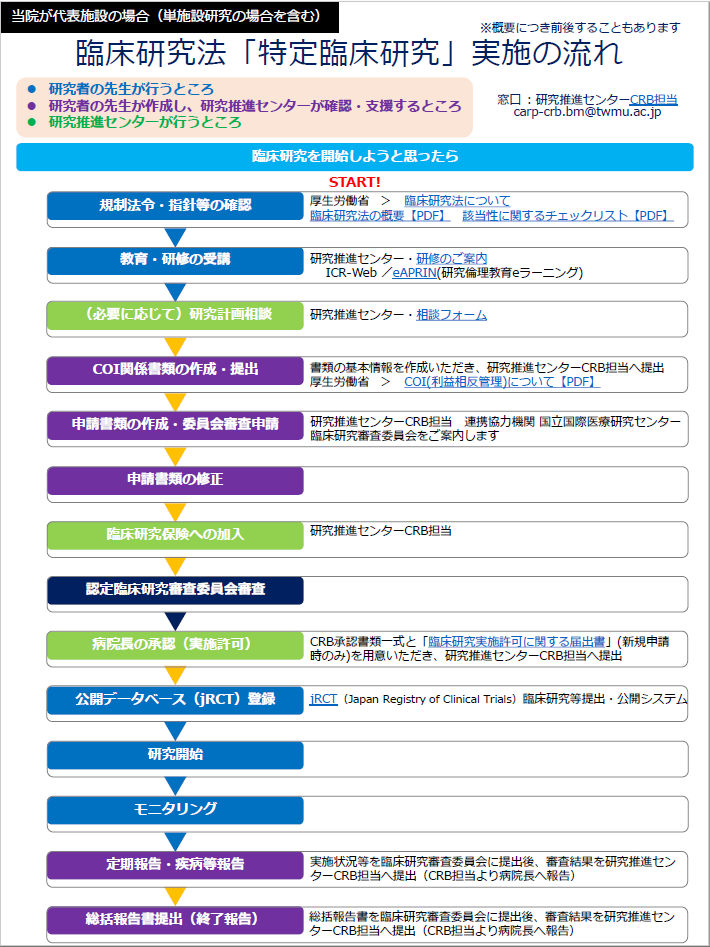
|
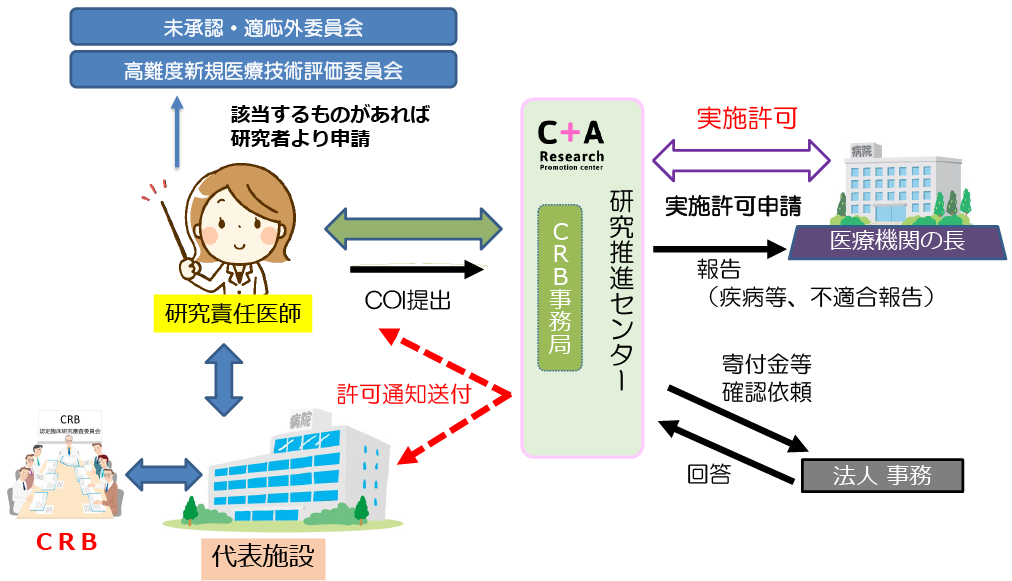
当院が分担施設の場合
当院が代表施設の場合(単施設研究の場合を含む)
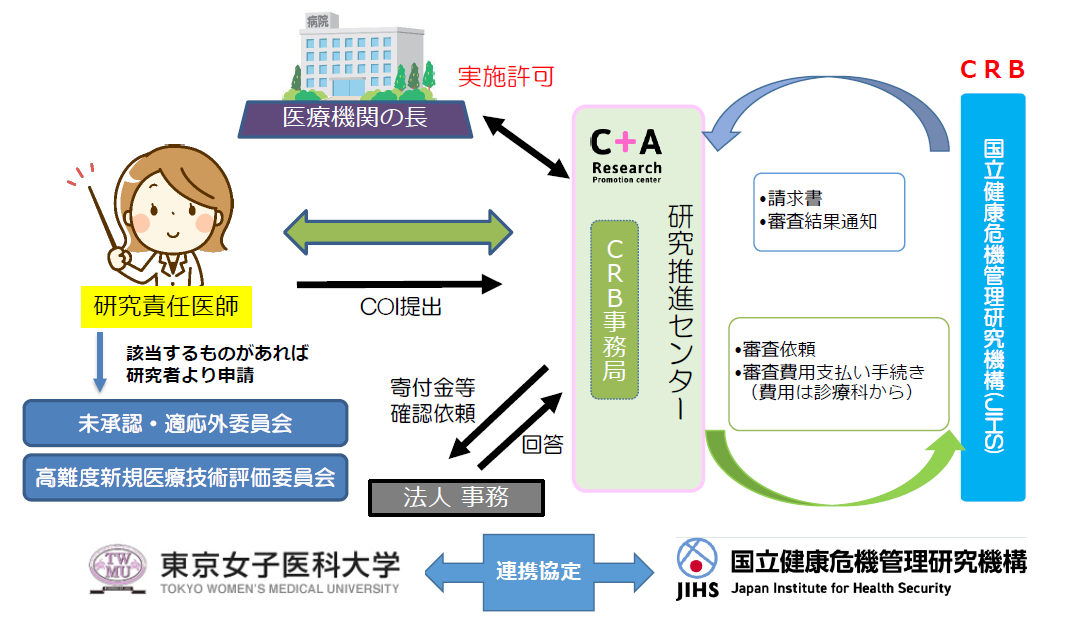
国立健康危機管理研究機構(JIHS)CRBへの審査申請に必要な登録を行います。
下の登録申請書に、研究責任医師と申請者の情報を記載し、メールでお送りください。








